PORANG
PORANG
Hallo, selamat sore, artikel ini akan membawakan mengenai porang bahasa jawa PORANG simak selengkapnya lebih dalam tentang PORANG.
PORANG
Potensi wilayah
Porang (Amorphophallus oncophillus) adalah golongan Araceae asli Indonesia yang banyak tumbuh secara liar di hutan-hutan pulau Jawa, sehingga di Jepang dikenal sebagai “Jawa Mukago Konyaku”. Porang merupakan tumbuhan semak (herba) dengan umbi di dalam tanah. Porang banyak tumbuh di hutan karena hanya memerlukan penyinaran matahari 50-60 % sehingga sangat cocok untuk tanaman di bawah naungan. Porang hanya memerlukan tanah kering berhumus dengan pH 6-7.
Kini tanaman porang banyak dibudidayakan di kawasan hutan Jawa Timur oleh masyarakat bekerjasama dengan Perum Perhutani Unit II. Sampai saat ini telah dikembangkan budidaya porang dengan luas areal mencapai lebih dari 1605,3 hektar, yang meliputi beberapa wilayah KPH yaitu Nganjuk 759,8 Ha, Saradan 615,0 Ha, Madiun 70,0 Ha, Bojonegoro 35,3 Ha, Jember 121,3 Ha dan Padangan 3,9 Ha (Data Perhutani Unit II Jawa Timur).
Selain porang terdapat sekitar 130 species lain dari golongan Amorphophallus dan banyak tumbuh di pegunungan daerah sub-tropis Asia. Di Indonesia selain porang (A. oncophyllus)
terdapat beberapa spesies lain, diantaranya adalah A.campanulatus, A. variabilis.
Kualitas bahan yang baik
-
Ciri-ciri umum tanaman porang yang siap dipanen : sebagian atau seluruh daun dan batang sudah mengering/mati (Ngripahi : bahasa jawa).
-
Cara pemungutan umbi : dengan menggali tanah di sekitar bekas batang (umbi yng menyembul, mungkruk : bahasajawa) dengan cangkul/gancu secara hati-hati, lalu umbi diangkat kepermukaan tanah.
-
Umbi yang dipanen dipilih hanya yang berukuran besar (minimal 1 Kg/umbi)dan sehat
-
Produksi umbi Porang berkisar antara 6-17 ton/ha (tergantung pada pemeliharaan). Tetapi pada umumnya rata-rata 9 ton/ha.
Ciri Fisik Dan Kimia
Ciri Fisik :
Berikut ini merupakan ciri-ciri fisik tanaman porang :




Batang tanaman porang
tegak, lunak, batang halus berwarna hijau atau hitam belang-belang (totol-totol) putih. Secara visual memang tidak terlalu berbeda dengan Suweg / Iles-iles Putih/ Walur (hanya saja kalau suweg kadang cenderung bercak gelap). Jika diraba baru terasa kalau kulit batang suweg terasa kasar.
Batang tunggal memecah menjadi tiga batang sekunder dan akan memecah lagi sekaligus menjadi tangkai daun. Pada setiap pertemuan batang akan tumbuh bintil/katak berwarna coklat kehitam-hitaman sebagai alat perkembangbiakan tanaman Porang. Tinggi tanaman dapat
mencapai 1,5 meter sangat tergantung umur dan kesuburan tanah.
Panjang tangkai daun porang berkisar 0,5 – 1,5 meter. Pada percabangan daunnya terdapat bulbil yang berwarna coklat. Bulbil merupakan umbi kecil berbentuk bulat yang berfungsi sebagai bibit pada jenis ini. Adanya tanda tersebut mempermudah identifikasi Amorphophallus oncophyllus Prain dari berbagai jenis lainnya. Panjang atmpuk bunga sekitar 12 – 125 cm, berwarna abu-abu dan berbintik-bintik kuning.
Ciri Kimia
Di Indonesia selain porang (A. oncophyllus)
terdapat beberapa species lain, diantaranya adalah A.campanulatus, A. variabilis. Analisa umbi yang meliputi warna kulit, warna daging, kadar glukomannan, diameter granula pati dan bentuk kalsium oksalat
Klasifikasi Berdasarkan Analisa Umbi Segar dari Amorphophallus
|
Analisa Umbi |
Spesies Amorphophallus |
||
|
campanulatus |
variabilis |
oncophyllus |
|
|
Warna kulit Warna daging Kadar glukomannan Diameter granula pati (mikron) Bentuk kalsium oksalat |
Coklat tua Oranye Tidak ada Agregat 20-30 Tunggal 10-15 Jarum |
Abu-abu Putih 10% – 15% Agregat 20-30 Tunggal 5-8 Jarum |
Coklat keabu-abuan Kuning kemerah-merahan 15 – 65% Agregat 20-30 Tunggal 2-3 Jarum |
Komposisi Kimia Umbi Segar dan Tepung Amorphophallus oncophyllus
|
Analisis |
Kandungan per 100 g conth (bobot basah) |
|
|
Umbi segar (%) |
Tepung (%) |
|
|
Air Glukomannan Pati Protein Lemak Serat berat Kalsium Oksalat Abu Logam berat (Cu) |
83.3 3.58 7.65 0.92 0.02 2.5 0.19 1.22 0.09 |
6.8 64.98 10.24 3.42 – 5.9 – 7.88 0.13 |
Sumber : Arifin (2001)
Senyawa Pembatas
Masalah utama yang dihadapi dalam pengembangan porang sebagai bahan pangan di Indonesia adalah adanya kalsium oksalat yang menyebabkan rasa gatal dan iritasi saat dikonsumsi. Selain penyebab rasa gatal dan iritasi, konsumsi makanan yang mengandung kalsium oksalat dapat menyebabkan kristalisasi dalam ginjal dan gangguan-ganguan kesehatan lainnya. Pemanfaatan umbi porang lebih lanjut membutuhkan teknologi untuk menghilangkan senyawa kalsium oksalat tersebut.
Masalah teknis yang berkaitan dengan penghilangan senyawa kalsium oksalat pada umbi porang berkaitan pula dengan fakta-fakta sebagai berikut:
-
Masa panen umbi porang yang sangat pendek (Juni – Agustus) dan sifat umbi porang yang mudah sekali busuk, sehingga umbi porang harus dikeringkan dalam bentuk chip dan disimpan dengan baik sebelum diolah lebih lanjut.
-
Metode pengolahan cara kering ini membuat chip porang yang dihasilkan menjadi sangat keras, komponen glukomanan dan non-glukomanan (pati, protein dan kalsium oksalat) menempel kuat satu sama lain. Akibatnya pemisahan antara fraksi glukomanan dan non glukomanan menjadi sulit.
-
Penepungan biasa dengan menggunakan hammer mill tidak dapat memecah matrik glukomanan dan non-glukomanan yang kuat tersebut. Penepungan dengan hammer mill yang dilanjutkan dengan pemisahan dengan hembusan udara menghasilkan tepung porang yang masih terasa gatal.
Oksalat terdapat dalam hampir semua bentuk bahan hidup. Pada tanaman, oksalat terdapat dalam bentuk garam terlarut (K, Na dan NH3 oksalat) dan sebagai asam oksalat atau sebagai Ca-oksalat tak larut. Asam oksalat dalam tanaman terbentuk di dalam cairan gel, berikatan dengan logam yaitu, kalium, natrium, amonium, atau kalsium membentuk garamnya. Asam oksalat bebas banyak dijumpai pada sejumlah tanaman, bukan merupakan produk dari siklus krebs. Senyawaan bebas ini beracun, tetapi biasanya dihilangkan dengan proses pemasakan (Paul and Palmer, 1972)
Asam oksalat dapat ditemukan dalam bentuk bebas atau dalam bentuk garam. Bentuk yang lebih banyak ditemukan adalah bentuk garam. Kedua bentuk asam oksalat tersebut terdapat baik di dalam bahan nabati maupun hewani. Akan tetapi terdistribusi dalam jumlah yang tidak merata. Dalam tanaman, asam oksalat terdapat dalam jumlah yang lebih besar, sementara itu bahan pangan hewani mengandung asam oksalat alami lebih rendah. Penyebaran asam oksalat pada tanaman bervariasi cukup besar antara famili tanaman yang satu dengan tanaman yang lain. Di dalam penyebaran yang sama, kandungan asam oksalat dapat bervariasi tergantung pada varietasnya. Demikian juga pada varietas yang sama kandungan oksalat bervariasi sesuai dengan kondisi tanaman. Distribusi asam oksalat pada bagian-bagian tanaman juga tidak merata. Daun pada umumnya mengandung asam oksalat lebih banyak dibandingkan dengan asam oksalat yang terdapat dalam tangkai, sedangkan dalam Poligonaceae, kandungan oksalat pada petiole hampir dua kali lebih besar daripada tangkai umumnya daun muda mengandung asam oksalat lebih sedikit dibandingkan dengan daun muda (Bradbury and Holloway, 1988).
Posisi kristal kalsium oksalat disajikan pada gambar berikut
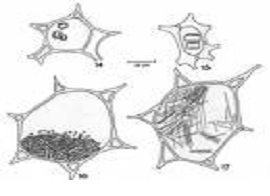
Bagian terbesar dari asam oksalat yang terkandung dalam tanaman adalah dalam bentuk oksalat yang larut (natrium dan terutama kalsium oksalat) dan hanya 10-20% merupakan kalsium oksalat yang tidak larut, terutama yang berada dalam sel. Fraksi oksalat yang larut akan bertambah besar dengan bertambah besarnya asam oksalat. Aging atau tanaman lewat masak biasanya diikuti oleh kenaikan proporsi kalsium oksalat dan bahkan terdapatnya krisal oksalat di dalam sel. Hal ini dapat digunakan sebagai petunjuk lewat masak pada pemanenan hasil (Bradbury and Holloway, 1988).
Jalur sintesa oksalat berbeda-beda, menurut Bradbury and Holloway (1988) oksalat merupakan konversi dari glycoxylate ke glyxylate dan glyoxylate baru ke oksalat. Fungsi kristal oksalat dalam tanaman kemungkinan sebagai pertahanan terhadap hama, cadangan Ca untuk perkecambahan dan pertunasan. Oksalat merupakan produksi ekskresi dari metabolisme yang cenderung menumpuk dengan meningkatnya umur.
Konsentrasi asam oksalat dalam dosis tinggi bersifat merusak dan menyebabkan gastroenteritis, shock, kejang, rendahnya kalsium plasma, tingginya oksalat plasma dan kerusakan jantung. Efek kronis konsumsi bahan pangan yang mengandung oksalat adalah terjadinya endapan kristal kalsium oksalat dalam ginjal dan membentuk batu ginjal (Bradbury dan Holloway, 1988). Kadar kalsium oksalat yang boleh dikonsumsi tiap orang menurut Siegelbaum (2008) sebesar 50 mg per hari.
Kristal Ca-oksalat bentuknya bervariasi dari tanaman satu ke tanaman lainnya, antara lain berbentuk seperti jarum, bunga karang, melintang seperti huruf H serta beberapa diantaranya tampak seperti berambut. Bentuk kristal ini terdistribusi dalam sel dibawah kendali genetik serta berperan khusus dalam fisiologis sel tanaman (Bradbury and Holloway, 1988). Berikut merupakan variasi bentuk kalsium oksalat yang paling umum dijumpai pada tanaman, yaitu dalam bentuk bunga karang (Gambar a) dan jarum (Gambar b).
Gambar a gambar b


Sumber : Sengbusch (2007)
Gambar 5. Variasi Bentuk Kalsium Oksalat pada Tanaman
Sedangkan beberapa sifat umum dari kalsium oksalat ditunjukkan pada Tabel berikut:
Sifat – sifat kalsium oksalat
|
Struktur umum kalsium oksalat |
|
|
Kelarutan dalam air |
0.00067 g/100 ml (20 °C) |
|
Suhu terdekomposisi |
189.5 °C |
|
Suhu tersublimasi |
157°C |
Sumber : Anonymous ( 2006a)
Metode Pemurnian Tepung Porang Secara Fisik
Pemanasan
Penghilangan senyawa oksalat secara fisik (pemanasan) yaitu penghilangan senyawa oksalat yang terdapat dalam umbi-umbian dengan cara perebusan dengan api yang besar sampai kulitnya dapat dikelupas (Hetterscheid, 1996). bahwa asam oksalat akan terdekomposisi akibat pemanasan. Kalsium oksalat akan mulai terdekomposisi pada suhu 101.5°C dan menyublim pada suhu 149 – 160°C (NIOSH, 2005).
Sentrifugasi
Sentrifugasi adalah pemisahan secara mekanis yang sering diaplikasikan oleh industry. Pemisahan secara mekanis ini bisa dilakukan dengan cara sedimentasi, sentrifugasi, dan atau filtrasi, tergantung pada bahan yang akan dipisahkan. Sentrifugasi merupakan pemisahan dengan cara diputar/dipusing dengan maksud memisahkan masa benda dengan berat jenis yang berbeda. Proses sentrifugasi ini biasanya ditemukan pada pembuatan tepung tapioka cara pabrik, dan pada pengolahan susu (Anonymous,2009a).
Tepung konjac yang dilarutan dalam air dapat membentuk suatu sistem koloidal. Senyawa-senyawa yang tidak larut dalam sistem koloid ini dapat dipisahkan dangan cara penyaringan ataupun dengan cara sentrifugasi. Senyawa pengotor tersebut akan mengendap dan terpisah dari larutan tepung konjac. Dengan demikian maka tingkat kemurnian dari tepung konjac akan meningkat (US Patent 3973008,1993).
Metode Pemurnian Tepung Porang Secara Kimiawi
Polisakarida secara alami umumnya berikatan dengan protein. Protein dan polisakarida membentuk suatu ikatan yang sangat menentukan kestabilan dari emulsi polisakarida dengan protein. Selain itu kondisi lingkungan juga sangat menentukan kestabilan dari ikatan protein dan polisakarida. Kondisi tersebut meliputi suhu, pH dan ikatan ionik. Penambahan bahan kimia mampu mengurangi kestabilan ikatan protein dan polisakarida. Sebagai contoh dengan penambahan polimer bermuatan negatif maka akan terjadi pengendapan protein (Blanshard and Mitchell,1979).
Alumunium Sulfat
Proses ekstraksi kotoran dari tepung konjac dilakukan dengan jalan memisahkan kotoran dari larutan tepung konjac, kemudian glukomanan yang terdapat dalam filtrat diendapkan dengan jalan penambahan alkohol selanjutnya dikeringkan dan digiling kembali. Metode ini memiliki beberapa keunggulan diantaranya adalah proses tidak membutuhkan waktu yang lama dan dapat menghasilkan produk yang murni dengan kelarutan yang tinggi, tidak bewarna, tidak berbau, dapat digiling menjadi ukuran yang seragam serta menghasilkan viskositas yang tinggi pula. Produk hasil pemurnian tepung konjac ini biasa disebut gum konjac dan dapat diaplikasikan secara luas dalam bidang pangan maupun farmasi (U.S Paten 2.144.5622,2000).
NaCl
Natrium klorida yang biasa dikenal sebagai garam, garam meja merupakan komponen kimia dengan formulasi NaCl. Natrium klorida yang menyebabkan tingginya tingkat salinitas air laut serta merupakan penyusun dari cairan ekstraseluler dari beberapa organisme multiseluler. NaCl biasa digunakan untuk pelengkap serta sebagai bahan tambahan makanan (Anonymous,2008a).
Isolasi glukomanan dapat dilakukan dengan cara mencampur tepung yang mengandung glukomanan kemudian dilarutkan dalam air yang bersuhu 70-80°C. Garam NaCl ditambahkan sebanyak 25% secara bertahap setiap 1 jam selama 7 jam. Kemudian dilakukan penyaringan. Untuk mengendapkan glukomanan maka ditambahkan alokohol dan dikeringkan (Mian and Timells,1960).
Tricloroacetat (TCA)
Asam trikloroasetat (nama sistematis: asam trikloroetanoat) adalah analog dari asam asetat, dengan ketiga atom
hidrogen dari gugus metil digantikan oleh atom-atom klorin. Senyawa ini merupakan asam yang cukup kuat (pKa = 0.77, lebih kuat dari disosiasi kedua asam sulfat). Senyawa ini dibuat melalui reaksi klorin dengan asam asetat bersama katalis yang cocok. Senyawa ini banyak digunakan dalam bidang biokimia, untuk pengendapan makromolekul seperti protein, DNA dan RNA. (Anonymous,2008b).
CH3COOH + 3Cl2 → CCl3COOH + 3HCl
Secara tradisional TCA digunakan dalam proses pengendapan protein. Umumnya digunakan untuk menentukan konsentrasi protein dengan cara pengendapan kuantitatif. TCA memiliki densitas 1,62 g/m suhu 25°C. TCA kelarutannya dalam air 0,5 M pada suhu 20°C membentuk larutan berwarna jernih (Anonymou,2008c).
Isolasi glukomanan dari umbi Eremurus zangezurticus dilakukan dengan cara mencampur tepung dari umbi ini dengan alkohol 80% kemudian dididihkan selama 1 jam. Kemudian dilakukan sentrifugasi selama 30 menit 2500 g. Endapan dibuang dan filtrat ditambahkan alkohol 96% dan disimpan dalam refrigerator selama 15 jam. Endapan dikumpulkan dan dilarutkan dalam air kemudian disentrifugasi lagi selama 20 menit 2500 g. Kemudian untuk mengendapkan protein ditambahkan TCA hingga konsentrasi 5% kemudian protein yang telah terdenaturasi dipisahkan dengan jalan sentrifugasi selama 30 menit 5000g. Filtrat bebas endapan ditambahakan alkohol 95% untuk mengendapkan glukomanan kemudian dikeringkan dan digiling. Hasil yang diperoleh merupakan glukomanan bebas potein (Irova, Mestechkina and Shcherbukhin, 2002)
Tepung konjac dimurnikan melalui pengendapan glukomanan dengan alkohol untuk membersihkan tepung konjac dari pati yang terlarut. Hasil dari proses pemurnian ini disebut gum konjac dimana kandungan poliglukomanannya mencapai 80%. Hidrokoloid jenis ini dapat digunakan secara langsung ataupun dapat dikombinasikan dengan xanthan gum, karagenan dan agen pengental yang lain dalam produk pangan. Setelah melalui tahapan pemurnian rendemen mengandung kadar gum yang tinggi dan senyawa yang tidak diinginkan dapat berkurang termasuk sulfurdioksida (Chan and Albert, 2008).
Ekstraksi glukomanan dengan alkohol memberikan keuntungan dimana senyawa karoteoid yang bercampur dengan glukomanan dapat diekstrak. Seyawa karotenoid akan larut dalam alkohol dan dipisahkan dari glukomanan (Chan and Albert, 2008)
Alkohol
Alkohol sering dipakai untuk menyebut etanol, yang juga disebut grain alcohol; dan kadang untuk minuman yang mengandung alkohol. Sebenarnya alkohol dalam ilmu kimia memiliki pengertian yang lebih luas lagi. Dalam kimia, alkohol (atau alkanol) adalah istilah yang umum untuk senyawa organik apa pun yang memiliki gugus hidroksil (-OH) yang terikat pada atom karbon, yang ia sendiri terikat pada atom hidrogen dan/atau atom karbon lain (Anonymous,2009b). Alkohol dapat digunakan untuk mengendapkan glukomanan yang telah dilarutkan dalam air (Rakhimov,Malikova and Zhauynbaeva, 2003).
Isolasi glukomanan kasar dapat dilakukan dengan cara mencuci tepung yang mengandung glukomanan dengan alkohol. Caranya dengan menambahkan alkohol dengan konsentrasi 80% pada tepung yang mengandung glukomanan kemudian dilakukan sentrifugasi untuk memisahkan glukomanan dengan senyawa-senyawa pengotor sehingga diperoleh endapan yang berwarna putih yang kemudian akan dikeringkan dan digiling (Mian and Timells,1960).
Air
Air merupakan kandungan penting dalam suatu bahan makanan. Air dapat berupa komponen intra sel dan atau ekstra sel dalam sayuran dan produk hewani, sebagai medium pendispersi atau pelarut dalam berbagai produk, sebagai fase terdispersi dalam mentega dan margarin, dan sebagai komponen tambahan dalam makanan lain (De Mann, 1997). Selain itu, air dapat berfungsi untuk menghilangkan senyawa oksalat. Namun senyawa oksalat yang dapat dihilangkan oleh air hanyalah senyawa oksalat yang berbentuk garam netral dengan logam alkali (Na, K), yakni sekitar 5 – 25% (Noor, 1992).
Metode produksi polisakarida konjac manan atau glukomanan meliputi prinsip dari kandungan tepung konjac, tepung konjac yang belum murni dihilangkan senyawa yang tidak larut dalam air dengan cara menyaring sol tepung konjac ataupun dengan perlakuan dialisis sehingga diperoleh hasil berupa filtrat yang kemudian dikeringkan dengan freezedrying namun produk yang dihasilkan sangat keras untuk digiling dan memiliki kelarutan yang rendah dalam air (Sugiyama et al, 1972).
Produk Olahan
Keripik dan Tepung umbi Porang
Pengolahan umbi iles-iles menjadi produk kering merupakan salah satu upaya untuk menekan aktifitas enzim yang merusak mannan. Manan di dalam umbi iles-iles harus dipertahankan kuantitas dan kualitasnya karena mannan ini merupakan komponen paling berharga yang terkandung dalam umbi iles-iles. Produk kering umbi iles-iles (antara lain kripik dan tepung) juga merupakan bentuk olahan yang lebih tahan disimpan, sehingga memudahkan transportasi, penanganan dan pendayagunaan selanjutnya.
Untuk mengubah umbi segar menjadi produk kering (khusus kripik), umbi harus diiris tipis-tipis (0.5 – 1.0 cm) dengan arah pengirisan tetap. Bila tebal irisan lebih kecil daripada 0.5 cm, menyebabkan umbi akan lengket pada alas tempat pengering, sehingga menyulitkan pengambilan kripik yang dihasilkan. Sedangkan bila tebal irisan melebihi 1.0 cm, menyebabkan proses pengeringan berjalan lambat dan kripik yang dihasilkan kurang baik. Kripik iles-iles ini sesungguhnya merupakan suatu produk yang nantinya digunakan lebih lanjut untuk bahan makanan atau bahan industri dan pihak pengimpor bagian besar juga menghendaki iles-iles dalam bentuk kripik.
Untuk memperoleh kripik yang baik diperlukan beberapa persyaratan, antara lain umbi segar yang bermutu baik, perlakuan pendahuluan yang baik, tebal irisan yang tepat dan seragam, teknik pengeringan yang intensif. Pendahuluan disini adalah dilakukan sebelum umbi dikeringkan. Untuk tujuan bahan makanan, perlakuan pendahuluan dimaksudkan untuk mengurangi jumlah rafida penyebab rasa gatal (kristal kalsium oksalat berbentuk jarum) dan alkaloid penyebab rasa pahit, yaitu konisin (conicine). Sedangkan untuk tujuan bahan baku industri, perlakuan pendahuluan dimaksudkan untuk mempertahankan mannan, baik kuantitas maupun kualitasnya sebelum mannan tersebut diekstrak dari umbi iles-iles.
Perlakuan pendahuluan yang umum dilakukan adalah perendaman irisan umbi di dalam air. Perlakuan ini tidak dapat menahan terjadinya pencoklatan pada kripik yang dihasilkan dan bahan sering menyebabkan penampakan kripik kurang menarik karena warna tidak seragam (bercak-bercak). Keadaan ini menyebabkan kripik iles-iles Indonesia sering ditolak oleh negara pengimpor. Untuk mengatasi masalah tersebut di atas, sebaiknya digunakan larutan garam dapur 5 persen sebagai larutan perendamnya. Fungsi garam dapur disini selain mencegah terjadinya pencoklatan dan penyeragam warna, juga sebagai penetral alkaloid, mempercepat pelarutan kalsium oksalat dan memperpanjang masa simpan kripik maupun tepung iles-iles yang dihasilkan.
Pengeringan irisan umbi yang telah diberi perlakuan pendahuluan dapat dilakukan melalui dua cara, yaitu cara penjemuran dan cara pengeringan buatan. Kedua cara pengeringan tersebut membawa keuntungan dan kerugian masing-masing. Cara dan sistem pengeringan berpengaruh terhadap mannan.
Cara penjemuran sifatnya lebih murah, mudah dan sering digunakan, tetapi memerlukan waktu yang lebih lama dan bergantung pada cuaca. Sedangkan cara pengeringan buatan sifatnya lebih mahal, tetapi jalannya proses dapat dikendalikan , sehingga kripik yang dihasilkan bermutu relatif baik.
Bila tebal irisan umbi 0.2 cm memerlukan waktu 16 jam dengan mempergunakan alat pengering oven pada suhu 70 oC. Sedangkan bila digunakan cara penjemuran untuk ketebalan irisan umbi 0,5 – 1,0 cm memerlukan waktu 30 jam efektif. Sebagai tanda bahwa kripik iles-iles telah kering dan siap digiling (ditumbuk) adalah bila kripik tersebut dipatahkan akan berbunyi “krek” atau bila kadar air kripik sekitar 12 persen berat basah. Pada kondisi tersebut diperkirakan semua mikroba tidak dapat tumbuh dan enzim-enzim sudah tidak efektif.
Tepung Mannan, Produk Utama Iles-iles
Untuk membuat tepung mannan dari kripik iles-iles telah dikenal dua cara, yaitu cara mekanis dan cara khemis. Untuk cara mekanis telah dikenal tiga cara, yaitu penggerusan dengan peniupan, penggerusan dengan pengayakan dan pengosokan. Sedangkan untuk cara khemis telah dikenal banyak cara, tetapi yang termudah adalah pengkristalan kembali dengan etanol.
Pada cara mekanis, umumnya kripik dijadikan tepung terlebih dahulu, kemudian baru dilakukan pemisahan berdasarkan bobot jenis dan ukuran molekul. Mannan merupakan polisakarida yang mempunyai bobot jenis dan ukuran molekul terbesar dan bertekstur lebih keras bila dibandingkan dengan molekul-molekul komponen tepung iles-iles lainnya. Karena bobot jenis molekul mannan lebih besar, maka dengan cara penghembusan (peniupan)
mannan akan jatuh terdekat dengan pusat “blower”, sedangkan komponen-komponen tepung lainnya (dinding sel, garam kalsium oksalat dan pati) akan jatuh lebih jauh. Demikian juga karena mannan mempunyai ukuran molekul lebih besar dan keras, dengan cara penyosohan oleh mesin “polisher” yang diperlengkapi dengan ayakan dan penghisap (ukuran lubang ayakan 0.5 – 0.8 mm) akan mengakibatkan fraksi kecil (dinding sel, garam kalsium oksalat dan pati) terhisap oleh penghisap, sedangkan mannan (fraksi besar) akan terkumpul tepat di bawah ayakan.
Cara kimiawi jarang dilakukan karena biayanya mahal dan membutuhkan peralatan yang lebih “complicated”, sehingga hanya digunakan untuk analisa pengukuran kadar mannan saja, baik mannan umbi segar, kripik ataupun tepung iles-iles.
Penggunaan atau Manfaat Glukomannan
Berdasarkan sifat-sifat tersebut di atas, glukomannan sangat berpotensi sebagai bahan baku berbagai macam industri. Beberapa penerapan glukomannan dalam bidang industri disajikan berikut ini.
Pembuatan Tablet
Pada pembuatan tablet dibutuhkan suatu bahan pengisi (filler) yang dapat memecah tablet di dalam lambung. Biasanya digunakan pati atau agar-agar yang mempunyai sifat pengembang di dalam air. Tetapi karena kristal glukomannan mempunyai sifat pengembangan yang lebih besar (sampai 200 persen), maka pemakaian glukomannan dalam pembuatan tablet akan memberikan hasil yang memuaskan. Hal ini disebabkan karena selain dapat menghancurkan tablet juga dapat berfungsi sebagai pengikat. Larutan
glukomannan mempunyai sifat merekat, sehingga memenuhi syarat sebagai pengikat dalam pembuatan tablet.
Penerapan sifat “film former” dari pada glukomannan digunakan untuk eknologi “film coating” dalam pembuatan “dragee” akan mempunyai prospek yang sangat cerah. “Film former” yang biasa digunakan adalah yang larut dalam pelarut organik (mudah menguap), sehingga sewaktu pelapisan akan erhirup oleh para pekerja. Sedangkan glukomannan adalah “film former” yang arut dalam air, sehingga pemakaiannya akan lebih digemari. Sifat glukomannan dalam pembentukan film yang larut ataupun tidak larut kembali bila dilarutkan dalam air, dapat digunakan sebagai bahan cat yang larut dalam air, tetapi bila dioleskan pada dinding timbul sifat tidak melarut kembali. Sifat idak melarut kembali yang dimiliki oleh glukomannan juga digunakan di dalam industri tekstil, yaitu untuk pencetakan (bila kering), pengkilapan dan ahan air. Sedangkan di dalam industri kertas, glukomannan digunakan sebagai pembuat kertas tipis, lemas, kuat dan tahan air.
Sifat glukomannan yang mirip dengan selulosa dapat digunakan sebagai pengganti selulosa di dalam industri pembuatan seluloid, isolasi listrik, film, bahan toilet dan kosmetika. Demikian juga sifat glukomannan yang mirip dengan agar-agar dapat digunakan di dalam bidang mikrobiologi (sebagai media penumbuhan mikroba) dan ternyata memberikan hasil yang sangat memuaskan. Akhirnya sifat larutan glukomannan encer yang dapat menggumpalkan suatu suspensi koloid dapat digunakan di dalam industri pertambangan, yaitu sebagai pengikat mineral yang tersuspensi secara koloidalpada hasil awal penambangan. Sifat ini juga digunakan di dalam proses penjernihan air minum yang berasal dari sungai, yaitu dengan cara pengendapkan lumpur yang tersuspensi dalam air sungai.
Sebagai ringkasan, berdasarkan sifat-sifat glukomannan, maka penggunaan atau manfaat zat tersebut antara lain :
Bahan Pembuat Lem
Berdasarkan sifat merekat dari pastanya, tepung mannan lebih baik jika dibandingkan dengan bahan perekat lainnya misalnya tepung beras. Pada suhu yang rendah daya rekatnya tidak hilang sehingga banyak digunakan dalam industri perekat kertas.
Pelapis Kedap Air
Tepung mannan juga dapat digunakan sebagai bahan dalam pembuatan alat-alat yang kedap air misalnya pembuatan tenda-tenda, jas hujan, payung dari kertas dsb.
Produk Makanan
Tepung mannan dapat dibuat makanan yaitu dengan pencampuran larutan mannan dan air kapur. Produk yang dihasilkan dikenal dengan nama “konnyaku” dan “shirataki”. “Shirataki” merupakan salah satu bahan untuk pembuatan makanan khas Jepang yaitu “Sukiyaki” yang sudah menjadi terkenal diberbagai negara. Di Indonesia produk “konnyaku” dan “shirataki” sudah dipasarkan pada beberapa toko swalayan di Jakarta, Bogor dan Surabaya. Jika dikonsumsi bahan makanan ini dapat berperan sebagai “dietary fiber” yang dapat menurunkan kadar kolesterol dalam darah.
DAFTAR PUSTAKA
Anonymous. 2006a. Konjac. www://en.wikipedia.org/wiki/Konjac .Tanggal akses 20 November 2010
Anonymous,2008a.Salting Out. . Tanggal akses 20 November 2010
Anonymous,2008b. TriChloro Acetate. . Tanggal 20 November 2010
Anonymou,2008c. Biochemichal and Reagent for Life Science Research. Merck
Anonymous,2009a. Pemisahan Mekanis pada Proses Pengolahan Pangan.. Tanggal akses 20 November 2010
Arifin, M. A.2001. Pengeringan Kripik Umbi Iles-iles Secara Mekanik Untuk Meningkatkan Mutu Keripik Iles-iles. Thesis. Teknologi Pasca Panen. PPS. IPB
Blanshard, J.M.V and Mitchell, J.R.1979. Polysaccharides in Food. Butterworths. Boson. London
Bradbury, O.H. and Holloway, 1988, Chemistry of Tropical Root Crops: Significance for Nutrition and Agriculture In The Pacific, Chemistry Department Australian Centre for International Agricultural Research, Canberra.
Chan and Albert, 2008. The world of food science Konjac Part I: Cultivation To Commercialization Of Component.New York
Hetterscheid, W. 1996. Amorphallus : Introduction And Toxonomic Description. International Aroid Society. . tanggal akses 15 Agustus 2006
Mian, Jabar and Timells T.E.1960. Isolation and Properties of a Glucomannan from the wood of Red Maple.Institute of Canada
N. I. Smirnova, N. M. Mestechkina and V. D. Shcherbukhin. 2002. Localization of Acetyl Groups in the Macromolecule of Glucomannan Obtained from Roots of Eremurus zangezuricus. Bach Institute of Biochemistry, Russian Academy of Sciences, Leninskii pr. 33, Moscow, 119071, Russia
NIOSH. 2005. Pocket Guide to Chemical Hazards, Oxalic Acid. Identification Number, RO2450000. National Institute for Occupational Safety and Health. New York
Noor, Z., 1992, Senyawa Anti Gizi, Pusat Antar Universitas Pangan dan Gizi, UGM, Yogyakarta
Paul, F. and J. Palmer. 1972. Chemistry Organic. Prentice Hall. London
U.S Patent 3973008,1993. Konjac Mannan. . Tanggal Akses 20 November 2010
US Patent 6162906, 2000. Clarified Konjac Glucomannan. akses 20 November 2010
U.S Patent 2.144.5622,2000. Clarified Konjac Glucomannan with Alumunium Sulfat. akses 20 November 2010
Sugiyama, N., Shimara, S and Ando, T. 1972. Studies on mannan and related
compounds I. The purification of konjac mannan. Bulletin Chem. Soc. Of Japan45:561-56
Begitulah detil perihal PORANG semoga artikel ini bermanfaat terima kasih
untuk pemesanan alat pengupaspencuci|pengolah} buah porang bisa menghubungi kami.
Artikel ini diposting pada tag porang bahasa jawa, umbi porang dalam bahasa jawa, umbi porang bahasa jawa,
https://lordbroken.wordpress.com/2010/12/04/porang/












Post Comment
No comments